
GASES
En este tema estudiaremos un gas hipotético formado por partículas puntuales sin atracción ni repulsión entre ellas y cuyos choques son perfectamente elásticos. La energía cinética es decir la energía del movimiento, es directamente proporcional a la temperatura en un gas ideal. Los gases reales que más se aproximan al comportamiento del gas ideal son los gases monoatómicos en condiciones de baja presión y alta temperatura.
Los gases ideales poseen las siguientes propiedades:
-
Las moléculas del gas se mueven a grandes velocidades de forma lineal pero desordenada
-
La velocidad de las moléculas del gas es proporcional a su temperatura absoluta
-
Las moléculas del gas ejercen presión sostenida sobre las paredes del recipiente que lo contiene
-
Los choques entre las moléculas del gas son elásticas por lo que no pierden energía cinética
-
La atracción / repulsión entre las moléculas del gas es despreciable

Ley de Boyle-Mariotte:
También llamado proceso isotérmico. Afirma que, a temperatura y cantidad de gas constante, la presión de un gas es inversamente proporcional a su volumen.




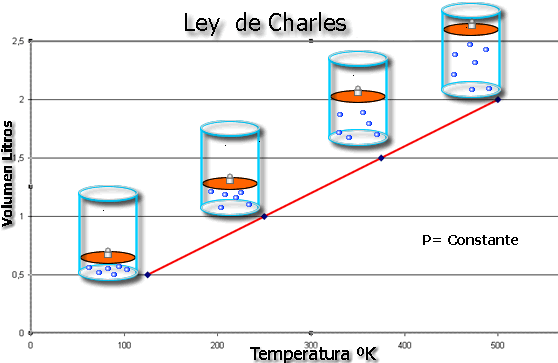
LEY DE CHARLES
La Ley de Charles es una ley de los gases que relaciona el volumen y la temperatura de una cierta cantidad de gas a presión constante. En 1787 Charles descubrió que el volumen del gas a presión constante es directamente proporcional a su temperatura absoluta (en Kelvin):


LEY DE GAY LUSSAC
Joseph Louis Gay-Lussac descubrió que a volumen constante, la presión del gas es directamente proporcional a su temperatura (en grados Kelvin).



ESCALAS DE TEMPERATURA
La temperatura es una medida que describe el movimiento interno de las moléculas de un material y se relaciona directamente con la energía cinética de las moléculas de este. Cuando la temperatura se incrementa, las moléculas de la sustancia se moverán con mayor velocidad, mientras que a menor temperatura, la velocidad de las moléculas disminuye.
La temperatura de un cuerpo es la misma en toda su superficie. En el Sistema Internacional la unidad de temperatura es el kelvin (K).
Escala de temperatura Celsius
Esta escala se basa en las temperaturas de congelación y ebullición del agua:
-
0 cuando se congela el agua;
-
100 cuando hierve el agua.
-
Esta escala se divide en cien intervalos iguales que llamamos grados. La escala Celsius es la más usada en el mundo. Los valores de temperatura menores al punto de congelación del agua son valores negativos, por ejemplo, la temperatura del congelador en el refrigerador esta entre -15 y -22 ºC.
Esta escala se llama así por el astrónomo sueco Anders Celsius (1701-1744).
Escala de temperatura Fahrenheit
En esta escala, la temperatura de congelación del agua es 32ºF (32 grados Fahrenheit) y la temperatura de ebullición del agua es 212ºF a la presión atmosférica estándar de una atmósfera de presión. Entre ambas lecturas hay 180 divisiones, o grados.
La escala Farehnheit es usada en los Estados Unidos, las islas Caiman, Bahamas y Belice. Fue propuesta por Daniel Gabriel Fahrenheit (1686-1736) en 1724, usando una mezcla de agua hielo y cloruro de amonio la cual se congela a 0ºF (-17,78 ºC), la temperatura de una mezcla de hielo y agua 32ºF y la temperatura del cuerpo humano 96ºF.
Escala de temperatura Kelvin
Llamada así por el físico inglés Lord Kelvin (1824-1907), esta escala se basa en la presión de los gases y se conoce también como la escala de temperatura absoluta. Un termómetro de gas muestra que la temperatura aumenta cuando la presión de un gas aumenta (en un volumen constante).
En una situación imaginaria donde la presión del gas es igual a cero, la temperatura en grados Celsius es -273,15 ºC. Esto se cumple para todos los gases, por eso el cero en la escala Kelvin corresponde a -273,15 ºC:
La escala de temperatura Kelvin es la unidad de medida de la temperatura en el SI y se abrevia K. En este caso NO se usa la palabra grado, simplemente kelvin, por ejemplo, el punto de congelación del agua es 273, 15 kelvins (K).


ACTIVIDAD
1.- Una cantidad de gas ocupa un volumen de 80 ml a una presión de 0,986 atm. ¿Qué volumen ocupará este gas a una presión de 1,2 atm si la temperatura no cambia?
2.- Disponemos de una muestra de gas que a 200°C presenta una presión de 2,8 atm y un volumen de 15,9 L. ¿Qué volumen ocupará este gas , si a la misma temperatura, la presión baja hasta 1,0 atm?
3.- Una cierta cantidad de gas ocupa un volumen de 200 mL a la presión de 0,986 atm. ¿Qué presión ocuparía este gas a un volumen de 50 mL a la misma temperatura?
4. - El volumen inicial de una cierta cantidad de gas es de 200 mL a la temperatura de 293,15 K. Calcule el volumen del gas si la temperatura asciende a 363,15 K y la presión se mantiene constante.
5.- Una masa de oxígeno ocupa 200 mL a 100°C. Determine su volumen a 0°C, si la presión se mantiene constante.
6.- Una cantidad fija de gas a 296,15 K ocupa un volumen de 10,3 Litros, determine la temperatura final del gas si alcanza un volumen de 23,00 L a presión constante.
7.- Una cierta cantidad de gas se encuentra a la presión de 790 mmHg cuando la temperatura es de 298,15 K. Determine la presión que alcanzará si la temperatura sube hasta los 473,15 K, si el volumen se mantiene constante.
8.- Se calienta aire en un cilindro de acero de volumen constante cuya temperatura y presión iniciales son 20°C y 3 atmósferas respectivamente. Determine la temperatura final del cilindro si la presión aumenta hasta 9 atmósferas.
9.- Una cierta cantidad de gas se encuentra a la presión de 790 mm Hg cuando la temperatura es de 25ºC. Calcula la presión que alcanzará si la temperatura sube hasta los 200ºC.