
PRESIÓN
La presión( P), es una magnitud física que mide la proyección de la fuerza en dirección perpendicular por unidad de superficie.
Presión de un gas
Teniendo en cuenta la teoría cinética (energía del movimiento), la presión de un gas es explicada como el resultado de las fuerzas implicadas por las colisiones de las moléculas del gas con las paredes del contenedor.
Para un gas ideal con (N) moléculas, cada una de ellas de masa (m) y moviéndose con una velocidad contenida en un volumen cúbico (V3).
Propiedades de la presión en un medio fluido
-
La fuerza asociada a la presión en un fluido ordinario en reposo se dirige siempre hacia el exterior del fluido, por lo que debido al principio de acción y reacción, resulta en una compresión para el fluido, jamás una tracción.
-
La superficie libre de un líquido en reposo (y situado en un campo gravitatorio constante) es siempre horizontal.
-
En los fluidos en reposo, un punto cualquiera de una masa líquida está sometida a una presión que es función únicamente de la profundidad a la que se encuentra el punto.


PRESIÓN DE VAPOR
La presión de vapor es la presión que ejerce la fase gaseosa o vapor sobre la fase líquida en un sistema cerrado a una temperatura determinada, en la que la fase líquida y el vapor se encuentran en equilibrio dinámico. Su valor es independiente de las cantidades de líquido y vapor presentes mientras existan ambas. Este fenómeno también lo presentan los sólidos; cuando un sólido pasa al estado gaseoso sin pasar por el estado líquido (proceso denominado sublimación o el proceso opuesto, llamado sublimación inversa o deposición) también hablamos de presión de vapor. En la situación de equilibrio, las fases reciben la denominación de líquido saturado y vapor saturado. Esta propiedad posee una relación directamente proporcional con las fuerzas moleculares, debido a que cuanto mayor sea el módulo de las mismas, mayor deberá ser la cantidad de energía entregada (ya sea en forma de calor u otra manifestación) para vencerlas y producir el cambio de estado. Observa la siguiente imagen y dibújala. Observa el video siguiendo el enlace debajo de la imagen.
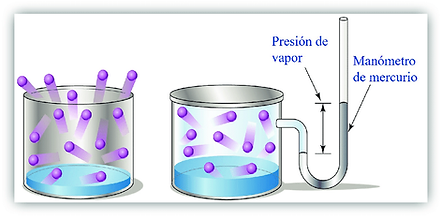

Presión atmosférica
¿Qué es la presión atmosférica?
La presión atmosférica o presión barométrica es la fuerza que ejerce la columna de aire de la atmósfera sobre la superficie terrestre en un punto determinado.
Esta fuerza es inversamente proporcional a la altitud. Cuando mayor es la altitud, menor en la presión atmosférica, y cuando menor es la altitud, mayor es la presión atmosférica.
La mayor presión atmosférica es la que se produce al nivel del mar. Por ende, esta medida se toma como referencia de la presión atmosférica normal.
Unidades de presión atmosférica
Existen diversas unidades de medida para representar la presión atmosférica. La utilizada en el S.I. es la llamada Pascal (Pa) o hectopascal (hPa). Sin embargo, también se usan bares (b), milibares (mb), “atmósferas” (atm), milímetros de mercurio (mm Hg) y Torricellis (Torr).
Fórmula de la presión atmosférica
La fórmula para calcular la presión atmosférica o barométrica se rige por los principios de la ecuación fundamental hidrostática. Veamos a continuación.
Pa = ρ.g.h
En esta fórmula,
-
Pa es igual a la presión ejercida en un punto del fluido.
-
ρ es igual a la densidad del fluido.
-
g es igual a la aceleración de gravedad.
-
h es igual a la profundidad.
De este modo, si:
-
ρ = 13550 kg/m3 (densidad del mercurio)
-
g = 9.81 m/s2
-
h = 0.76 m (altura de la columna de mercurio)
Entonces,
-
Pa = 101 023 Pa
Valor de la presión atmosférica al nivel del mar
El valor de la presión atmosférica normal (al nivel del mar) es de 760 mm, lo cual equivale a 760 torr; a 1.013,2 mb (milibares); 101 325 Pa (pascales); a 1013,2 hPa (hectopascales) o también a 1 atm (atmósfera).


Variación de la presión de vapor con la temperatura
Como una tendencia general, la presión de vapor de los líquidos a presión atmosférica se incrementa con el aumento en la temperatura de ebullición. Este fenómeno es ilustrado en el diagrama adjunto, que muestra, para varios líquidos, el comportamiento de su presión de vapor versus la temperatura. Por ejemplo, a cualquier temperatura, el clorometano (cloruro de metilo) tiene la más alta presión de vapor de todos los líquidos expuestos en el gráfico.


TALLER DE APRENDIZAJE
-
Explica en qué consiste el concepto de presión y en cuáles unidades se expresa.
-
Dibuja el experimento de Explica Torricelli explica en qué consiste.
-
Explica con tus palabras en qué consiste la presión de vapor de un líquido dibuja y da un ejemplo.
-
Dibuja la gráfica de presión y temperatura para el compuesto acetato de metilo. Cuál es la presión de esta sustancia a 25°C?. A 0,5 atm cuál es la temperatura que presenta el acetato de metilo?. Qué presión presenta el cloruro de metilo a 50 grados centígrados?
-
Explica qué es la presión atmosférica y cómo se comporta según la altura. Dibuja.

